国科大纳米科学与技术学院纳米生物学实验室在炎症性肠病治疗领域取得新进展
- 纳米科学与技术学院
- Created: 2022-11-15
炎症性肠病(IBD),包括溃疡性结肠炎(UC)和克罗恩病(CD),是一种慢性复发性炎症性消化系统疾病,主要表现为腹泻、腹痛、便血、体重减轻等症状,严重影响着人们的日常生活质量。IBD患者的肠道微环境遭破坏,包括活性氧 (ROS)水平升高、肠道菌群紊乱、免疫失调等直接导致肠道黏膜损伤,而目前临床的治疗策略靶点单一,难以全面恢复肠道内稳态平衡,根治IBD。近年来,以微生物为基础的疗法,如粪便移植和益生菌等,在恢复IBD患者肠道内稳态方面表现出优越性,然而这些策略的临床缓解率不足且缺乏特异性调控。此外,活菌的应用还会带来如内毒素、体内抗原变异等风险。因此,亟待发展以微生物为基础新方法,特异性调节肠道微环境稳态,安全有效的治疗IBD。
在前期研究工作中,中国科学院大学张银龙课题组与国家纳米科学中心聂广军研究员课题组及其合作者通过硒代胱胺偶联透明质酸(HA),开发了一种具有ROS清除活性的和靶向特性的功能性材料-纳米水凝胶(SeNG)。SeNG首先通过HA与炎症细胞表面高表达的CD44高效结合,介导其在结肠炎症部位的特异性富集。SeNG可通过直接清除ROS和上调Nrf2/HO-1信号通路两条途径共同降低靶细胞ROS水平,最终实现IBD的高效治疗(ACS Nano. 2022, 16(8), 13037-13048)。
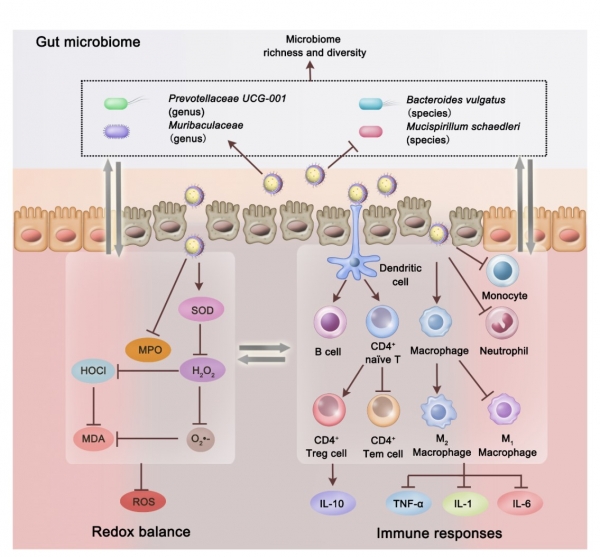
近日,在上述工作的基础上,该合作团队构建了一种益生菌启发的纳米药物(命名为SeM@EM),通过类后生元组分大肠杆菌Nissle1917-(EcN)膜(EM)包裹在联硒介孔二氧化硅纳米颗粒(SeM)表面,在右旋糖酐硫酸钠(DSS)诱导的小鼠结肠炎模型中,SeM@EM不仅能有效富集于肠道黏膜层,还能综合调节氧化还原平衡、结肠固有层免疫反应,此外有效增加肠道菌群多样性及丰富度,调整菌群结构,从而修复受损的上皮组织的紧密连接蛋白,实现结肠炎高效治疗的目的(图1)。由天然来源的类后生元组分益生菌膜包覆生物活性内核制备的纳米药物可以作为预防和治疗IBD安全有效的手段,并为治疗胃肠道及相关炎症性疾病提供新的研究思路。相关研究成果以Probiotic-inspired nanomedicine restores intestinal homeostasis in colitis by regulating redox balance, immune responses, and the gut microbiome为题,发表在Advanced Materials杂志上。(Adv. Mater. 2022, DOI: 10.1002/adma.202207890)。
图1.粘附于肠道粘膜的SeM@EM通过调节氧化还原平衡、固有层免疫反应,调控肠道微生物以缓解DSS诱导的急性结肠炎
中国科学院特别研究助理徐嘉琪博士为文章的第一作者,中国科学院大学张银龙副教授、国家纳米科学中心聂广军研究员、哥伦比亚大学Kam W Leong教授、华南理工大学邵丹教授为共同通讯作者。上述成果得到了国家重点研发计划、国家自然科学基金、中国科学院前沿科学重点研究计划、中央高校基本科研业务费专项资金等资助。
中国科学院大学张银龙课题组长期致力于疾病治疗纳米药物的开发,包括炎症性疾病、肿瘤及心血管疾病等,以解决重大恶性疾病诊疗面临的瓶颈问题。